Sert su
Suyun içerisinde bir takım iyonlar vardır. Bu iyonlar Kalsiyum ve magnezyum iyonlarıdır ve suda sertliğe neden olur.
Yağmur Suları yeraltında ve yerüstünde ilerlerken kireçli topraktan geçtiklerinde kireci çözerler. Bunun sonucunda suya Ca+2 iyonları karışır. Benzer şekilde bazı toprak katmanlarından da sular geçtiklerinde bu sulara Mg+2 iyonları da karışır. Yapısında Ca+2 veya Mg+2 veya her iki iyonu da fazla miktarda bulunduran sulara sert su denir.
Yumuşak – Sert Sular ve Sağlığa Etkileri
Sertlik terimi, suda bulunan polivalan iyonlar sayısını, özellikle kalsiyum ve magnezyum miktarını belirtmek için kullanılır. Ne var ki bu terim yetersiz kalmaktadır.
Sert sular, sağlığa doğrudan zararlı olmasa bile yemek pişirmeye ve içmeye elverişli değillerdir. Ayrıca bu nitelikteki su, çamaşır yıkamada ya da sanayide kullanılırsa, çok sabun sarfına neden olacağı gibi kazan ve boruların içine kireç tabakasının yığılmasına da yol açar.
Sulardaki sertlik iki türlüdür. Bikarbonatların oluşturduğu “geçici sertlik” ve kalsiyum ve magnezyum sülfatların oluşturduğu “kalıcı sertlik”tir.
Suyun sertliğini gidermek için; toz halinde kireç ya da soda (kalsiyum karbonat) kullanılır. Kireç, geçici sertliği, soda, kalıcı sertliği giderir. Bu amaçla evlerde ve sanayi kuruluşlarında, içinde sodyum alüminyum bulunan vebolit, permutit gibi iyon değiştirme aygıtları kullanılır.
Sert Suların Özellikleri;
1. Yapısında Ca+2 veya Mg+2 iyonu fazladır.
2. Kireçli su olarak da adlandırılırlar.
3. Sağlık açısından tehlikeli değildirler.
4. Ca+2 iyonu kemik gelişimi açısından faydalıdır.
5. Rengi şeffaf olabilir.
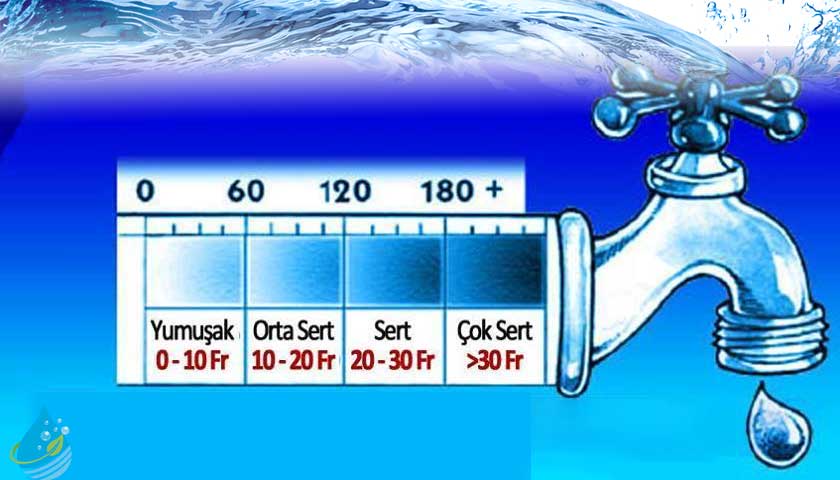
Suya Sertliği Veren Maddeler Ve Sertlik Derecesi
Suların içinde erimiş halde bulunan kalsiyum ve magnezyum tuzlarından kaynaklanan sertlik (acılık), suyun içme, endüstri ve hizmet alanında kullanımı için önemli bir kalite özelliğidir.
Kalsiyum ve magnezyum bikarbonat tuzları Ca(HCO3)2 ve Mg(HCO3)2 “geçici sertliği” veya “karbonat setliğini”, kalsiyum ve magnezyumun klor, sülfat, nitrat, fosfat ve silikat tuzları ise “kalıcı sertliği” meydana getirirler. Kalıcı ve geçici sertlik birlikte “toplam sertliği” veya “genel sertliği” oluştururlar. Genel olarak “karbonatlar geçici sertliği, sülfatlar kalıcı sertliği verirler” denir.
Suların sertlik derecesini ölçülebilmesi için kullanılan pratik yöntem, sabun solüsyonu yöntemidir. Bu yöntemde; sertliği veren Ca ve Mg elementleri, sabundaki Na ve potasyumun yerine geçerek suda erimeyen bileşikler yapar. Herkes tarafından bilinen sert suların, zor köpürmesinin nedeni budur. Sabun solüsyonu kullanarak, suda devamlı bir köpük elde edilmeye çalışılır. Bu işlemde harcanan sabun solüsyonu miktarı genel sertlik hakkında bilgi verir. Su kaynatıldıktan sonra, yine aynı yöntemle kalıcı sertlik ölçülebilir. (Geçici sertlik = Genel sertlik – Kalıcı sertlik) formülü kullanılarak geçici sertlik hesaplanabilir.
Yumuşak sulara göre sert sularla yıkanan çamaşırlar, daha fazla sabun gerektirmektedir. Bununla birlikte sertlikle ilişkili yapı suda fazla sabun kullanımımı azaltacak ekonomik yapıya ilişkili bir sınır değer yoktur. Sentetik deterjanların geliştirilmesi ile birlikte bunların içerdiği yumuşatıcı maddeler sertliği ekonomik problem olmaktan zaten çıkarmıştır.